9 Задачи по электрохимии часть 4
Задача К146
Проведены испытания бетона в условиях агрессивной среды. По результатам испытаний установлено, что количество корродированного цементного камня в пересчете на CaO, отнесенное к площади регулирующией поверхности бетона, при выдержке в течении 9 суток составляет 0,003 г/см2, при выдержке в течении 25 суток – 0,008 г/см2. Рассчитать экспериментальный коэффициент К интенсивности коррозии [г/(см2*сут0,5].
Скачать решение задачи К146 (цена 100р)
Задача К147
Вода, поступающая в стальной трубопровод со скоростью 4 л/мин, содержит 5,5 мл О2 на литр воды. Вода, выходящая из трубопровода содержит 0,05 мл О2 на литр. Рассчитайте скорость коррозии в г/м2*сут, принимая, что коррозия полностью протекает на нагретом участке трубопровода площадью 3 м2 с образованием Fe(OH)2.
Скачать решение задачи К147 (цена 100р)
Задача К148
Как измениться предельный расчетный срок эксплуатации плотины из бетона класса W 0,2, если ее толщину увеличить в 2 раза. Действующий напор воды составляет 20 м.в.ст. Бетон изготовлен с использованием портландцемента с содержанием CaO 50%. Расход цемента в бетоне Ц = 300 кг/м3.
Скачать решение задачи К148 (цена 100р)
Задача К149
Предложить технические мероприятия по защите железобетонных фундаментов промышленного здания контактирующих с грунтовыми водами (рН=6,5), содержащими: хлорид ионы 5 мг/л, сульфат ионы 2,5 г/л, ионы калия 0,5 г/л, ионы железа 0,5 г/л. Пользуясь СНиП 2.03.11-85 обосновать предложенные мероприятия
Скачать решение задачи К149 (цена 100р)
Задача К150
Определить степени окисления каждого элемента в следующих соединениях KNO2, Cr2(SO4)3, Cl2
Скачать решение задачи К150 (цена 100р)
Задача К151
Расставить коэффициенты в следующих уравнениях методом ионно-электронного баланса (методом полуреакций): KMnO4 + HCl = Cl2 + KCl + MnCl2 + H2O
Скачать решение задачи К151 (цена 50р)
Задача К152
Запишите уравнения электролитической диссоциации следующих электролитов в водном растворе и определите значение изотонического коэффициента при бесконечном разбавлении раствора: Ва(NO3)2, FeCl2, Na3PO4.
Скачать решение задачи К152 (цена 80р)
Задача К153
Рассчитать степень диссоциации в следующих растворах слабых электролитов, пользуясь справочными данными Кдисс.(для многоосновных кислот учитывайте только первую ступень диссоциации) 0,05 М раствора сероводородной кислоты (Кдисс.= 6,0•10-8).
Скачать решение задачи К153 (цена 100р)
Задача К154
Определить ионную силу раствора смеси LiNO3 (0,01 M), K2S (0,05 M), Na3PO4 (0,02 M).
Скачать решение задачи К154 (цена 70р)
Задача К155
Напишите уравнения электродных процессов на катоде и аноде, происходящих при электролизе водного раствора соли на угольных электродах: CsI, MnCl2, Li2CO3, CuBr2.
Скачать решение задачи К155 (цена 60р)
Задача К156
При изучении реакции между пиридином и йодистым этилом
С5H5N + C2H5I = C7H10N+ + I-
измерялась концентрация ионов I- через определенные промежутки времени. Для одиннаковых концентраций двух исходных реагентов (со = 0,1М) были получены следующие данные:
t, с 235 465 720 1040 1440 1920 2370
c(г), М 0,085 0,074 0,065 0,056 0,048 0,041 0,036
Определите порядок и вычислите константу скорости реакции
Скачать решение задачи К156 (цена 100р)
Задача К157
По значениям констант скоростей к1 = 0,00125 и к2 = 0,105 при двух температурах Т1 = 288К и Т1 = 313К определить:
- энергию активации,
-константу скорости реакции к3 при температуре Т3 = 365К,
- температурный коэффициент константы скорости реакции у,
- период полупревращения (период полураспада),
-концентрацию реагентов к моменту времени t = 10мин при температуре Т3, если исходная концентрация С0 = 1,55 моль/л.
NaBO3+H2O = NaH2BO3 + 1/2O2
Скачать решение задачи К157 (цена 100р)
Задача К158
Для реакции, протекающей в гальваническом элементе, дано уравнение зависимости ЭДС от температуры (по вариантам в таблице). При заданной температуре Т = 295К, вычислить ЭДС Е = 0,869 – 6,5*10-4*T, изменение энергии Гиббса, изменение энтальпии, изменение энтропии, теплоту, выделяющуюся или поглощающуюся в этом процессе. Расчет произвести для 1 моля реагирующего вещества:
Cd + 2AgCl = CdCl2 + Ag
Скачать решение задачи К158 (цена 100р)
Задача К159
Составьте гальванический элемент, чтобы в нем протекали следующие реакции и рассчитайте ЭДС в стандартных условиях. Рассчитайте константу равновесия окислительно-восстановительной реакции
Ad2O + HCOH = 2Ag + HCOOH
Скачать решение задачи К159 (цена 100р)
Задача К160 (3)
Будет ли выпадать в осадок при добавлении к 100 мл 0,02 и раствора сульфата калия 100 мл 0,01 и раствора хлорида кальция? ПР (CaSO4) = 2,5*10-5
Скачать решение задачи К160 (цена 100р)
Задача К161 (9)
Каково содержание CaO (% мас.) в известняке, если при опрелении кальция из нарезки 0,3025г получено 0,2505г осадка CaSO4 (гравиметрическая форма. Мол. масса (CaO) 56,08; мол масса (CaSO4) 136,14
Скачать решение задачи К161 (цена 100р)
Задача К162 (15)
Вычислите рН раствора, полученного смешенного 19 см3 6,2 н. раствора уксусной кислоты и 1 см3 2,0 н. раствора ацетата натрия.
Скачать решение задачи К162 (цена 60р)
Задача К163 (21)
Вычислите рН 2,14%-го раствора хлорида аммония (р=1 г/см3), K(NH3*H2O) = 1,8*105
Скачать решение задачи К163 (цена 50р)
Задача К164 (Задание 1)
Как происходит коррозия цинка, находящегося в контакте с медью при водородной и кислородной деполяризации в: а) кислом, б) щелочном растворах
Скачать решение задачи К164 (цена 70р)
Задача К165 (Задание 2)
Напишите схему гальваничнеского элемента, состоящего из аллюминиевого и медного электродов. Определите полюсы элемента, напишите процессы, идущие на электродах при работе данного элемента.
Скачать решение задачи К165 (цена 60р)
Задача К166 (Задание 3)
Исходя из величины энергии Гиббса при стандартных условиях, определите, какие из металлов будут корродировать во влажном воздухе по уравнению
Ме + Н2О + О2 = Ме(ОН)n
Ме = Ва, Cu
Скачать решение задачи К166 (цена 100р)
Задача К167 (Задание 4)
Определить массу цинка, перешедшего в раствор в результате анодного процесса за один час при плотности коррозионного тока 100 А/м2. Найти скорость коррозии, если известно, что площадь анодных участков 0,01 м2.
Скачать решение задачи К167 (цена 100р)
Задача К168 (Задание 5)
При взаимодействии магния с кислородом образуется оксидная пленка состава MgO. Определить, способна ли она защищать металл от коррозии (pMg = 1,74 кг/м3, pMgО = 3,2 кг/м3)
Скачать решение задачи К168 (цена 100р)
Задача К169
Концентрационная константа диссоциации NH4OH в водном растворе при 25°С равна 1,79*10-5. При какой концентрации степень диссоциации NH4OH равна 0,02 и чему равна концентрация ионов ОН-
Скачать решение задачи К169 (цена 50р)
Задача К170
Определить константу гидролиза цианида натрия и рН нго водного раствора при концентрации 0,01 моль*кг-1 и температуре 25°С, если полное произведение воды и термодинамическая константа диссоциации цианистоводородной кислоты равны 1*10-14 и 7,9*10-10 соответственно.
Скачать решение задачи К170 (цена 50р)
Задача К171
Рассчитать средний коэффициент активности раствора, содержащего 1 ммоль *л-1 MgSO4 при 298,2 К, использую уравнение первого приближения теории Дебая – Хюккеля
Скачать решение задачи К171 (цена 80р)
Задача К172
Вычислить величину ионной силы для раствора, содержащего 1 л раствора 0,01 моль CaCl2 и 0,1 моль Na2SO4
Скачать решение задачи К172 (цена 80р)
Задача К173
Применяя предельный закон Дебая и Хюккеля, вычислить значение коэффициента активности для 0,01 м раствора Ba(OH)2. Коэффициент А уравнения Дебая и Хюккеля для воды при этих условиях равен 0,54.
Скачать решение задачи К173 (цена 100р)
Задача К174
Вычислить рН раствора, если ЭДС, двойной (концентрационной) цепи с хингидронными электродами равна 0,232В при 18°С
Скачать решение задачи К174 (цена 80р)
Задача К175
Рассчитать переходное время катодного восстановления комплекса цинка из его 0,001 моль/л раствора при плотности тока 2 А/дм2, если коэффициент диффузии ионов цинка равен 2*10-5 см2/с.
Скачать решение задачи К175 (цена 80р)
Задача К176
Стандартные токи обмена при 20°С для кобальта в растворах CoSO4, CoCl2 и CO(NO3)2 соответственно равны 13*10-5, 2*10-7, 6,3*10-8 А/см2. Определить величины поляризации электрода в этих растворах, если плотность тока электроосаждения кобальта равна 10-6 А/см2.
Скачать решение задачи К176 (цена 100р)
Задача К177
Рассчитать величину диффузионного перенапряжения при анодном растворении цинка для плотности тока 1 мА/см2 при температуре 18°С в электролите, содержащем 10-3 г-экв ZnSO4 в 1 см3. Для ионов Zn2+ в указанном растворе: коэффициент активности равен 0,063; коэффициент диффузии – 0,72*10-5 см2/с, число переноса - 0,4. Эффективную толщину диффузионного слоя б с естественной конвекцией принять равной δ = 0,075см.
Скачать решение задачи К177 (цена 80р)
Задача К178
Рассчитать предельный ток диффузии по ионам при электролизе 0,001 моль/л раствора ZnSO4, содержащего электрохимический инертный сульфат натрия, если коэффициент диффузии разряжающихся ионов равен 2*10-5 см2/с, а толщина диффузионного слоя для конвективно не перемешиваемого раствора составляет 0,075 см.
Скачать решение задачи К178 (цена 80р)
Задача К179
Вычислить при 25°С ЭДС следующего элемента;
(+) Cd [CdCl2 ][ZnCl2] Zn(-)
2м 0,005м
Стандартные электродные потенциалы Cd2+/Cd и Zn2+/Zn соответственно равны – 0,402 и – 0,763 В. Средние коэффициента активности CdCl2 и ZnCl2 в растворах, указанных концентраций равны 0,044 и 0,789. Диффузионный потенциал на границе электролитов не учитывать.
Скачать решение задачи К179 (цена 100р)
Задача К180
Золь иодида серебра получен смешением равных объемов иодида калия и нитрата серебра. Пороги коагуляции у (моль/дм3) для различных электролитов имеют следующие значения: Ca(NO3)2 – 315, NaCl – 300, MgCl2 – 320, Na3PO4 – 0,6, Na2SO4 – 20, AlCl3 – 330. Какой из электролитов: иодид калия или нитрат серебра взят в большей концентрации для приготовления золя? Дайте обоснованный ответ
Скачать решение задачи К180 (цена 100р)
Задача К181
Требуется приготовить 322 г 34% раствора едкого натра из растворов содержащих 6% и 69% NаОН. Рассчитать исходное количество растворов. Сколько необходимо взять 63% раствора Н2SО4 для нейтрализации полученного раствора. Составить материальный баланс.
Скачать решение задачи К181 (цена 50р)
Задача К182
Сколько необходимо взять 63% раствора Н2SО4 для нейтрализации полученного раствора.
2NaOH + Н2SО4 = Na2SО4 + 2Н2O
Скачать решение задачи К182 (цена 50р)
Задача К183
В результате 20-летних испытаний образцов никеля оказалось, что средняя скорость коррозии составила 0,037 мм/год, для городской атмосферы и 0,002 мм/год для сельской атмосферы. Рассчитайте скорость 23 коррозии в г/(м·сут), плотность никеля 8,91 г/см3.
Скачать решение задачи К183 (цена 100р)
Задача К184
Провести модифицирование катализатора методом пропитки из 25% водного раствора тетрагидрата сернокислого марганца в количестве 0,2% масс. Навеска катализатора равна 250г
Скачать решение задачи К184 (цена 100р)
Задача К185
Площадь поверхности 10-6 м3 активированного угля равна 1600 м2. Какой объем аммиака могут адсорбировать 25·10-6 м3 активированною угля, если принять, что вся поверхность полностью покрыта мономолекулярным слоем аммиака? Условно можно считать, что поперечное сечение молекулы NH3 представляет собой квадрат с длиной стороны 2·10-10 м и что при полном заполнении поверхности соседние молекулы касаются друг друга.
Скачать решение задачи К185 (цена 100р)
Задача К186
Провести декатнокирование цеолитного катализатора (массой 100 г, плотностью 0,63 г/см куб) трехкратной обработкой 2 %-ным раствором хлорида аммония. Рассчитать количество воды и соли для приготовления пропиточного раствора.
Скачать решение задачи К186 (цена 100р)
Задача К187
Определите молекулярную рефракцию нитробензола при 298 К на основании справочных данных о его показателе преломления и плотности.
Скачать решение задачи К188 (цена 100р)
Задача К188
Показатель преломления и плотность пропилового эфира хлормуравьиной кислоты при 298 К равны 1.4035 н 1.090•103 кг/м3. Определите молекулярную рефракцию и сопоставьте ее с рассчитанной по правилу аддитивности.
Скачать решение задачи К189 (цена 100р)
Задача К189
Определите молекулярную рефракцию глицерина С3Н5(ОН)3 в воде при 293 К. если показатель преломления 10%-ного раствора 1.34481. его плотность 1.0221•103 кг/м3. Показатель преломления воды 1.33303, плотность воды 1.0006* 103 кг/м3.
Скачать решение задачи К189 (цена 100р)
Задача К190
(6) Рассчитать количество сорбента, достаточное для очистки 27 м3 сточных вод, содержащих 82 мг/л ионов меди (II), если емкость сорбента до проскока при работе в динамическом режиме составляет 147,4 г/л (коэффициент запаса сорбента принять равным 1,3). Определить количество 10 % раствора серной кислоты, необходимое для регенерации этого количества сорбента, если ионы меди (II) сорбируются в виде гидроксида меди. Найти концентрацию ионов меди в элюате после регенерации.
Скачать решение задачи К190 (цена 100р)
Задача К191
(10) Предприятие сбрасывает азотнокислые стоки в количестве 200 м3/сутки, содержащие 6,3 кг/м3 азотной кислоты. Какое количество извести необходимо для нейтрализации кислотных стоков? Товарный продукт содержит 50 % СаО.
Скачать решение задачи К191 (цена 100р)
Задача К192
(13) Для определения железа в воде колориметрическим методом в две мерные колбы емкостью 25,00 мл ввели в первую 6,00 мл и во вторую 9,00 мл стандартного раствора железа (ТFe = 0,0100 г/мл), в третью колбу - 20 мл испытуемого раствора. После добавления соответствующих реактивов были определены оптические плотности растворов на фотоэлектроколориметре: А1 = 0,33; А2 = 0,63; Ах = 0,51. Вычислить содержание железа в анализируемой воде в мг/л.
Скачать решение задачи К192 (цена 100р)
Задача К193
(14) На титрование 200 мл воды из Невы было затрачено 2,25 мл 0,1 н раствора KMnO4 (К=0,8466). Вычислить окисляемость воды и сделать вывод о загрязнении ее восстановителями, если норма окисляемости по кислороду 7,6 мг/л.
Скачать решение задачи К193 (цена 100р)
Задача К194
(15) Предельно допустимая массовая концентрация ионов меди в воде составляет 0,1 мг/л. Для очистки промышленных стоков от ионов Cu2+ осаждают гидроксид меди (II) добавлением щелочи. Какое значение рН при 25 С необходимо поддерживать в растворе для снижения содержания ионов меди до предельно допустимого?
Скачать решение задачи К194 (цена 100р)
Задача К195
(16) Промышленные стоки некоторого предприятия содержат серебро (в виде ионов Ag+). Перед их сбросом проводится осаждение AgCl при 25 С и концентрации ионов Cl– равной 0,001 моль/л (предельно допустимое содержание ионов Cl– в пресной воде). Какая масса (г) серебра рассеивается в окружающую среду за год работы этого предприятия, если дебит сброса 1000 л/сутки? Эффективен ли данный способ очистки?
Скачать решение задачи К195 (цена 100р)
Задача К196
(17) 50 м3 сточных вод гальванического цеха содержат сульфат железа (II) с концентрацией 15,2 кг/м3. Для осаждения железа используется 0,1 н раствор щелочи. Определить объем раствора щелочи, необходимый для осаждения железа.
Скачать решение задачи К196 (цена 100р)
Задача К197
(18) В каком объемном соотношении необходимо смешать кислотные стоки, содержащие 4,9 кг/м3 серной кислоты, и щелочные стоки, содержащие 56 кг/м3, для их взаимной нейтрализации.
Скачать решение задачи К197 (цена 100р)
Задача К198
(19) Для определения аммонийного азота навеску удобрения массой 2,635 г растворили в мерной колбе вместимостью 250 мл. К 25,00 мл полученного раствора добавили формальдегид, выделившуюся кислоту оттитровали 18,72 мл раствора NaOH (T(NaOH) = 0,003987). На титрование формальдегида в холостом опыте израсходовали 0,5 мл NaOH. Вычислить массовую долю азота в удобрении (в %).
Скачать решение задачи К198 (цена 100р)
Задача К199
(20) Схема пылеосадительной камеры:
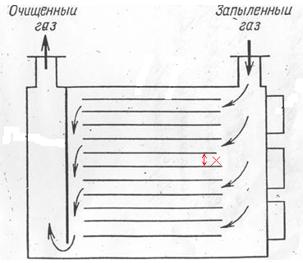
Рассчитать Х , если известны:
|
№ |
Параметры камеры д × ш × в, м |
Характеристики проходящего газа |
Характеристика пылевых частиц |
||||
|
Расход (при н.у.), м3/с |
Т, оС |
µ (при Т), мПа*с |
Плотность (при Т), кг/м3 |
Диаметр, мкм |
Плотность (при Т), кг/м3 |
||
|
1 |
3,9х2,8х4,0 |
0,45 |
392 |
0,029 |
0,48 |
6 |
3500 |
Скачать решение задачи К199 (цена 100р)
Задача К200
Производительность аммиачного завода 34 т в сутки. Какой минимальной емкости должны быть газгольдеры для водорода и азота для того, чтобы последних было не менее двухчасового запаса?
Скачать решение задачи К200 (цена 100р)
Задача К201
Напряжение на серии алюминиевых электролизеров, соединенных последовательно, 396 В, сила тока 165 кА, выход по току 84%. Рассчитать производительность серии, удельный расход электроэнергии, выход по энергии и периодичность загрузки глинозема в ванны, если напряжение на ванне 4,3 В, напряжение разложения Al2O3 - 1,5 В, единовременная порция загрузки глинозема в ванну 150 кг, машинное время работы ванн 0,96. Расчет произвести на год.
Скачать решение задачи К201 (цена 100р)
Задача К202
Образцы сшитого полимера характеризуются следующими значениями молекулярной массы отрезка между поперечными сшивками 600, 15000, 30000, 60000. Каково соотношение между температурами стеклования этих образцов полимера, если молекулярная масса механического сегмента равна 30000?
Скачать решение задачи К202 (цена 100р)
Задача К203
Подсчитать, какой будет для стекла SuW высота столба раствора K2CrO4 в 5-ной H2SO4, соответствующая по окраске 2,7 (концентрация K2CrO4 0,002341%).
Скачать решение задачи К203 (цена 100р)
Задача К204
Рассчитайте весовой показатель коррозии, если изменение массы металла за промежуток времени τ на поверхности металла площадью S = 300м2, равна Δm = 50 г,.
Чему равен глубинный показатель коррозии для листов металла, если глу-бина проникновения коррозионного разрушения в тело металла равна σ = 52мм за время τ = 850 час. Исходя из этих параметров, найдите «теоретическую плотность» металла.
Скачать решение задачи К204 (цена 100р)
Задача К205
Концентрация электролита Na3PO4 0,0006 моль/кг. Рассчитайте ионную силу этого раствора.
Скачать решение задачи К205 (цена 100р)
Задача К206
Рассчитайте критерий Бэтфорда и на его основе дайте характеристику оксидной пленки
Металл Fe
Плотность 7,87 г/см3
Оксид FeO
Плотность 18,5 г/см3
Скачать решение задачи К206 (цена 100р)
Задача К207
Определите толщину оксидной пленки в случае кинетического контроля и диффузионного, если известно время образования пленки t, константа скорости, концентрация кислорода на поверхности пленки и константа диффузии
k*10-5 С0, моль/м2 kд*10-15 Время t, час
3,2 0,23 20,7 700
Скачать решение задачи К207 (цена 100р)
Задача К208
Методом полуреакций подобрать коэффициенты в окислительно-восстановительном уравнении. Указать процессы окисления и восстановления, какое вещество является окислителем, восстановителем.
FeSO4 + HNO3 + H2SO4 → NO + H2O + Fe2(SO4)3
Скачать решение задачи К208 (цена 100р)
Задача К209
В 1 л 1,4 М раствора KI при 20 °С растворяли добавочный иодид калия. Определите среднюю движущую силу растворения после того, как в раствор перешло 10 моль иодида калия, если при этой температуре растворимость KI составляет 144 г на 100 г воды
Скачать решение задачи К209 (цена 100р)
Задача К210
Концентрация электролита Na3PO4 0,0006 моль/кг. Рассчитайте ионную силу этого раствора.
Скачать решение задачи К211 (цена 100р)
Задача К211
Вычислить адсорбцию масляной кислоты на поверхности раздела водного раствора с воздухом при 273К и концентрации 0,5 кмоль/м3, если зависимость поверхностного натяжения от концентрации выражается уравнением Шишковского: σ=σ0-16,7*10-3LN(1+21,5c). Поверхностное натяжение воды при этой температуре 72,75·10-3 Дж/м2. Построить изотерму адсорбции и определить A.
Скачать решение задачи К211 (цена 150р)
Задача К212 (2.24)
По следующим данным вычислить полную поверхностную энергию для бензола и сделать вывод о зависимости полной поверхностной энергии от температуры
Температура, К 363 383 413 433
G*10-3 , Н/м 19,16 16,85 14,45 11,29
Температурный коэффициент dG/dT Н/(м*К) -0,113 -0,1155 -0,111 -0,108
Скачать решение задачи К212 (цена 150р)
Задача К213 (3.24)
Рассчитайте и постройте интегральную и дифференциальную кривые распределения частиц веселовской глины в воде, пользуясь графическим методом обработки кривой седиментации.
t, мин 0,25 0,5 1 2 4 8 12 16 24 28
m, мг 2 7 11 14 22 37 45 48 50 50
Высота оседания Н = 0,12 м; вязкость n = 1*10–3 Па с; плотность глины p = 2,54*103 кг/м3; плотность дисперсионной среды 1*103 кг/м3. Использовать метод построения касательных к кривой седиментации.
Скачать решение задачи К213 (цена 150р)
Задача К214 (4.24)
Как изменится растворимость и реакционная способность порошкообразного молибдена, если средний размер частиц составит 10 мкм и 10 нм при температуре 298 K? Поверхностное натяжение составляет 2,19 Дж/м2.
Скачать решение задачи К214 (цена 150р)
Задача К215 (6.24)
Используя уравнение БЭТ, постройте изотерму адсорбции бензола по нижеуказанным данным и рассчитайте удельную поверхность адсорбента по изотерме адсорбции бензола:
P/Рs 0,03 0,07 0,12 0,17 0,24 0,31 0,38
А, моль/кг 0,196 0,301 0,373 0,423 0,488 0,52 0,625
Скачать решение задачи К215 (цена 150р)
Задача К216 (7.24)
Работа когезии воды WК = 145,5*10–30 Дж/м2. Краевой угол смачивания тефлона, граничащего одновременно с воздухом и водой, θ = 120°. Чему равна работа адгезии на границе тефлон – вода?
Скачать решение задачи К216 (цена 100р)
Задача К217
V1 мл спиртового раствора скипидара (концентрация раствора равна 10 кг/м3) добавили раствор стабилизатора. Общий объем смеси равен V2.
Показатель преломления среды n0 равен 1,332.
Длина волны падающего света λ0 равна 540 нм.
Толщина кюветы l = 3 см.
Используя задания, приведенные в каждом из вариантов (V1,V2, плотность скипидара ρф, показатель преломления скипидара n, оптическую плотность системы D), а также исходные данные:
а) рассчитайте весовую концентрацию с (в кг/м3) скипидара;
б) определите мутность системы;
в) найдите длину волны падающего света в дисперсионной среде (λ) по формуле λ = λ0/n0;
г) рассчитайте средний объем частицы скипидара в эмульсии по уравнению Рэлея;
д) вычислите средний радиус частиц скипидара;
е) рассчитайте частичную концентрацию скипидара.
Вар 1 V1 = 0,1*10-6 м3, V2 = 50*10-6 м3, рф = 0,85*103 кг/м3, n = 1,46, D = 0,02.
Скачать решение задачи К217 (цена 100р)
Задача К218
Рассчитайте коэффициент диффузии коллоидного золота при 20°С в воде, если радиус его частиц равен 10-9 м, вязкость равна 0,001 Н·с/м2
Скачать решение задачи К218 (цена 100р)
Задача К219
Удельная поверхность сферических частиц гидрозоля кремнезема составляет 1,1·106 м2/кг. Плотность кремнезема 2,7 г/см3, вязкость дисперсионной среды 10-3 Па·с, температура 293 К. Определите проекцию среднего сдвига частиц золя за время 4 с.
Скачать решение задачи К219 (цена 100р)
Задача К220
Определить удельную поверхность молекулярных сит, используя экспериментальные данные сорбции углекислого газа при 256К.
Равновесное давление р*10-2, Н/м 25 50 100 150 200 300 500
Г*103, кмоль/кг 3,64 3,83 3,94 4,03 4,10 4,19 4,27
Давление насыщенного пара Ps=23,7•105 н/м2, молярный объем углекислого газа V = 0,0354 м3/кмоль. При, расчете пользоваться уравнением Дубинина для сорбентов I структурного типа.
Скачать решение задачи К220 (цена 150р)
Задача К221
Из наблюдений смещения частиц гуммигута вычислить константу Авогадро, если радиус частиц равен 0,0212 мкм, а за время, равное 1 мин. частицы переместились на 10,65 мкм. Температура опыта 17°С, вязкость среды 0,011 Пуаза.
Скачать решение задачи К221 (цена 150р)
Задача К222 (Задание 1)
Определить общий экономический ущерб от загрязнения воздуха в рабочем поселке промышленными выбросами.
Исходные данные:
- среднегодовая концентрация пыли составляет 0,3 мг/м3;
- среднегодовая концентрация SO2 составляет 0,2 мг/м3;
- численность населения в поселке составляет 6500 человек;
- сельскохозяйственных угодий 250 га;
- стоимость основных производственных фондов составляет 550 млн. рублей;
- стоимость очистки промышленных выбросов составляет 657520 рублей.
Скачать решение задачи К222 (цена 100р)
Задача К223 (Задание 2).
Определить ущерб здравоохранению и промышленности, наносимый отдельным предприятием при выбросе пыли, SO2 и СО.
- количество выбросов в год: пыли – 6 тыс. т, SO2 – 2 тыс.т, СО – 11 тыс. т;
- численность населения по зонам (Ч): зона 1– 8 тыс. человек, зона 2 – 6 тыс. человек;
- высота трубы (h) – 160 м;
- стоимость производственных фондов (Ф) составляет 75 млн. рублей.
- стоимость очистки промышленных выбросов (О) составляет 40682 рублей.
Скачать решение задачи К223 (цена 100р)
Задача К224 (Задание 3)
Определить количество секций мелкозернистого фильтра, используемого для очистки производственных сточных вод.
Исходные данные:
- максимальный часовой расход производственных сточных вод составляет qw=3460 м3/ч;
- содержание взвешенных частиц веществ и БПКполн в биологически очищенной сточной воде соответственно Сen=35 мг/л и Len=30 мг/л;
- содержание взвешенных веществ и БПКполн в воде после глубокой очистки должно быть Сex=20 мг/л и Lex= 25 мг/л. Станция очистки работает круглосуточно.
Скачать решение задачи К224 (цена 100р)
Задача К225 (Задание 4)
Определить оптимальные параметры септика, используемого для очистки сточных вод.
- суточный расход хозяйственно-бытовых сточных вод предприятия составляет Q = 11 м3/сут;
- концентрация взвешенных веществ в стоках составляет Cen = 280 мг/л;
- значение БПКполн равно Len = 310 мг/л;
- норма водоотведения составляет a = 170 л/(сут·чел).
Скачать решение задачи К225 (цена 100р)
Задача К226 (Задание 5)
Рассчитать параметры аэротенка - смесителя с регенератором для очистки сточных вод I ступени второй системы канализации нефтеперерабатывающего завода.
– расход поступающей на очистку воды Qв = 1000 м3/ч;
– БПКполн поступающей в аэротенк сточной воды Len = 300 мг/л;
– БПКполн очищенной воды Leх = 110 мг/л;
– степень регенерации Rr = 0,3;
– иловый индекс I = 100 см3/г;
– средняя доза ила а = 3,5 г/л;
– концентрация ила в осветленной воде t = 20 мг/л;
– концентрация растворенного кислорода С0 = 2 мг/л;
– среднегодовая температура сточных вод tв = 14 °С.
Скачать решение задачи К226 (цена 100р)
Задача К227 (Задание 6)
Определить экономический эффект, получаемый при очистке сточных вод.
- расход сточной воды Q = 14000 м3/сут;
- исходная концентрация загрязняющих веществ в сточной воде, С1 = 2200 мг/л;
- концентрация загрязняющих веществ после очистки, С2 = 125 мг/л;
- максимальная концентрация загрязняющих веществ в водоеме, ПДКм = 128 мг/л;
- капитальные затраты на очистку сточных вод, К = 140 тыс. руб.;
- эксплуатационные затраты на очистку сточных вод, С = 19 тыс. руб.;
- удельный показатель предотвращенного ущерба, У = 1440 руб./год;
- число рабочих дней в году, N = 245;
- предельно допустимая концентрация (ПДК) загрязняющих веществ в водоеме, мг/л:
взвешенные частицы 5
кислород (по БПК полн.) 5
сульфаты 500
аммиак 0,05
Скачать решение задачи К227 (цена 100р)
Задача К228
Оценить величину предотвращенного ущерба при переводе химического комбината на малоотходную технологию.
Исходные данные:
- объем сточных вод Q = 17 млн. м3/год;
- место расположения комбината на р. Дон (устье р. Воронеж)
- содержание загрязняющих веществ в сточных водах, С, мг/л:
до очистки после очистки
взвешенные частицы 150 51
кислород (по БПполн.) 65 20,8
сульфаты 90 42
аммиак 0,72 0,15
- предельно допустимая концентрация (ПДК) загрязняющих веществ в водоеме, мг/л:
взвешенные частицы 4
кислород (по БПК полн.) 5
сульфаты 500
аммиак 0,05
Скачать решение задачи К228 (цена 100р)
Задача К229 (Задание 7)
Определить размеры факельной трубы для разгрузки предохранительных клапанов при следующих исходных данных: давление газа в сбросной трубе (Р) 100 кПа; температура окружающего воздуха (t) 200°С; характеристика выброса (G) углеводороды 173601 кг/ч, водяной пар 24199 кг/ч.
Скачать решение задачи К229 (цена 100р)
Задача К230 (Задание 8)
Определить выбросы вредных веществ, при регенерации шарикового катализатора на установке каталитического крекинга, и оценить ущерб от загрязнения атмосферы.
– производительность установки G= 20 т/ч;
– объем подаваемого на регенерацию воздуха V = 23000 м3/ч;
– содержание серы в сырье установки Sс = 0,0035 масс. доли;
– масса катализатора М = 73 т,
– содержание кокса на катализаторе до регенерации С1 = 0,0054 масс. доли, после регенерации – С2= 0,0006 масс. доли;
– температура газов на выходе из регенератора Т = 200°С;
– безразмерный показатель σ =4,3.
Скачать решение задачи К230 (цена 100р)
Задача К231 (Задание 9)
Оценить экологический ущерб от загрязнения атмосферы выбросами котельной и предложить варианты по защите и уменьшению количества выбросов сажи в атмосферу.
– среднегодовая температура наружного воздуха tн = -6°C;
– среднегодовая температура выбрасываемой газовоздушной смеси tсм = 198°C;
– высота трубы котельной h = 13 м;
– фактический выброс сажи Gc = 16,8 т/год;
– среднегодовой модуль скорости ветра V = 0.55 м/с;
– общая зона загрязнения Sоб. = 18 км2 из них, территория предприятия Sпр = 30 %, населенный пункт Sнп = 40 %, лес Sл = 30 %;
– удельный экологический ущерб от выброса 1т вредных веществ в атмосферу γ = 192 руб/усл. т.
Скачать решение задачи К231 (цена 100р)
Задача К232
Кабельный полиэтилен (плотность 921 кг/м3) содержит 0,65 масс. долей полиэтилена «НД» и 0,35 масс. долей полиизобутилена. Определить расход (кг) полиэтилена для обеспечения непрерывной работы в течение 8ч шнек-машины производительностью 20000 м/ч. Кабель – круглая медная проволока диаметром 5*10-4 м с толщиной покрытия 4*10-4 м.
Скачать решение задачи К232 (цена 100р)
Задача К233 (24)
Рассчитайте время оседания в воде частиц песка размерами 10-5 и 10-8 м с высоты 0,1 м. Плотность песка 2 г/см3, плотность дисперсионной среды 1 г/см3, вязкость дисперсионной среды при температуре 293 К 10-3 Па·с. Оцените седиментационную устойчивость дисперсных систем.
Скачать решение задачи К233 (цена 100р)
Задача К234
В соответствии с заданным вариантом (табл.1) произвести расчет рассеивания нагретого выброса указанного в таблице вредного вещества из высокого одиночного источника с круглым устьем (труба) в атмосфере.
Таблица 1 Исходные данные
Вредное вещество NO2, Н = 40м, Тг = 135 °С, Тв = 30 °С, D=1,2м, w0=10м/с, М = 10 г/с, ПДКм.р.=0,085
Скачать решение задачи К234 (цена 100р)
Задача К235
В соответствии с заданным вариантом (табл.1) произвести расчет рассеивания холодного выброса указанного в таблице вредного вещества из высокого одиночного источника с круглым устьем (труба) в атмосфере.
Вредное вещество NO2, Н = 40м, D=1,2м, w0=10м/с, М = 10 г/с, ПДКм.р.=0,085
Скачать решение задачи К235 (цена 100р)
Задача К236
Рассчитать циклон в соответствии с заданным вариантом (табл. 1). Материал пыли - известняк, Плотность частиц р = 2650 кг/м3, Степень полидисперсности пыли lgG=0,384, Расход газа Q = 0,4 м3/с. Концентрация пыли на входе циклона Свх = 0,78 г/м3.
Скачать решение задачи К236 (цена 100р)
Задача К237
Постройте изотермы адсорбции и десорбции водяного пара на пшеничном глиадине в координатах Г = f(р/рs), по максимальной величине сорбции рассчитайте общую пористость сорбента, пользуясь данными:
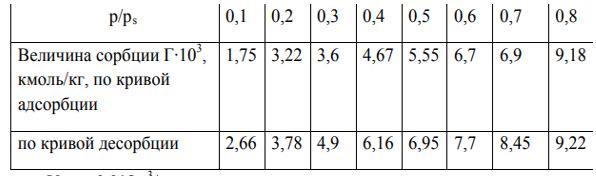
Скачать решение задачи К237 (цена 200р)
Задача К238
Вычислить адсорбцию валериановой кислоты на поверхности раздела водный раствор-воздух при 293 К и концентрации 0,0206 кмоль/м3, если известна зависимость поверхностного натяжения от концентра-ции раствора :
с, кмоль/м3 0 0,0103 0,0206 0,0683 0,2049
g, Дж/м2 72,53 65,45 59,78 49,31 35,20
Скачать решение задачи К238 (цена 150р)
Задача К239
По экспериментальным данным сорбции углекислого газа на активированном угле A построить изотерму адсорбции и определить константы уравнения Фрейндлиха:
P*102, Н/м2 5 10 30 50 75 100
A*103, кмоль/кг 3,0 5,5 16,0 29,0 31,0 35,0
Вычислить величину сорбции газа при давлении 250 Н/м2.
Скачать решение задачи К239 (цена 150р)
Задача К240
При изучении адсорбции в системе «вода-изоамиловый спирт» при температуре 296 К получены экспериментальные данные по величинам поверхностного натяжения:
c, кмоль/м3 0,008 0,016 0,031 0,062 0,125 0,250 0,500
G, Дж/м3 0,0699 0,0670 0,0642 0,0612 0,0583 0,0554 0,0525
Определить константы уравнения Ленгмюра, если при температуре 296 К поверхностное натяжение воды составляет 72,28·10-3 Дж/м2.
Скачать решение задачи К240 (цена 150р)
Задача К241
Найти величину С-потенциала на границе кварцевое стекло – 0,001 М водный раствор KCl. Процесс электроосмоса характеризуется следующими данными: сила тока I=4*10-4 A, время переноса V=10-8 м3, раствора t =12,4 секунды, удельная электрическая проводимость среды x =1,8*10-2 См*м-1, вязкость среды n = 1*10-3 Н*с/м2, диэлектрическая проницаемость среды е = 81.
Скачать решение задачи К241 (цена 100р)
Задача К242
Рассчитать величину С-потенциала для латекса полистирола по следующим данным: при электрофорезе смещение а цветной границы за время t = 60 минут составляет 2,5·10-2 м. Напряжение, приложенное к электродам, U = 115B, расстояние между электродами L =0,55 м.
Скачать решение задачи К242 (цена 100р)
Задача К243
Рассчитать и построить кривую распределения суспензии песка в анилине по экспериментальным данным о количестве осевшей суспензии, % во времени (секунды):
t, с 60 300 600 1200 1800 3000 4200
Q, % 12,9 55,2 73 86,5 92,3 98 100
Плотность песка 2,1·103 кг/м3, плотность анилина 1,02·103 кг/м3, вязкость анилина 4,43·10-3 Н·с/м2, высота раствора 0,12·м
Скачать решение задачи К243 (цена 200р)
Задача К244
При исследовании гидрозоля золота с помощью ультрамикроскопа подсчитано 5 частиц в объеме V=12*10-19 м3. Приняв форму частиц за шарообразную, рассчитать их средний радиус (r) и удельную поверхность золя (Sуд), если концентрация золя c =30*10-2 кг/м3, плотность золота p = 19,3*103 кг/м3.
Скачать решение задачи К244 (цена 100р)
Задача К245
Написать формулу золя Sb2S, стабилизованного SbCl3. Указать, какой из добавленных электролитов KBr, Ba(NO3)3, K2CrO4 и AlCl3 имеет наименьший порог коагуляции?
Скачать решение задачи К245 (цена 100р)
Задача К246
К = 3·10-4 м3 0,1% раствора KCl добавлено 1·10-4 м3 0,01 кмоль/м3 раствора AgNO3. Для изучения коагуляции к полученному золю AgCl добавлены следующие электролиты: NаCl, Ca(NO3)2 и AlCl3. Какой из добавленных электролитов имеет наименьшую коагулирующую способность?
Скачать решение задачи К246 (цена 100р)
Задача К247
По уравнению Ленгмюра вычислить Г и площадь, приходящуюся на одну молекулу пропилового спирта на поверхности раздела водный раствор - воздух, если известны постоянные уравнения Шишковского А = 14,4·10-3 и В = 6,6 при температуре 293К.
Скачать решение задачи К247 (цена 100р)
Задача К248
При исследовании аэрозолей методом поточной ультрамикроскопии в объеме 1,33·10-11 м3, протекшим через счетное поле микроскопа, подсчитано 50 частиц масляного тумана. Определить средний радиус частиц, приняв их форму за сферическую. Концентрация аэрозоля 2,5·10-6 кг/м3, плотность масла 0,9*103 кг/м3.
Скачать решение задачи К248 (цена 100р)
Задача К249
Золь бромида серебра получен смешением равных объемов растворов KBr и AgNO3. При коагуляции золя для различных электролитов получены следующие значения порогов коагуляции (cm, моль/м3): Ca(NO3)2 - 315; NaCl - 300; MgCl2 - 320; Na3PO4 - 0,6; Na2SO4 - 20; AlCl3 - 330. Какой из электролитов, KBr или AgNO3, имел большую концентрацию при приготовлении золя?
Скачать решение задачи К249 (цена 200р)
Задача К250
Определить поверхностную активность этого ПАВ, если поверхностное натяжение воды при этой температуре равно 72,75·10-3 Дж/м2.
Скачать решение задачи К250 (цена 100р)
