По Балыбердину вар 1 и 2
Вариант 1 пример 1
Задача 1 (вар 1). Определить карбонатную, некарбонатную и общую жесткость воды заданного состава, а также массу фосфата натрия (Na3PO4 * 12H2O), необходимого для ее умягчения.
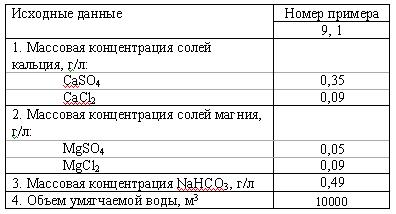
Скачать решение задачи 1 (вар 1) (цена 70р)
Задача 2 (вар 1). Комплексное удобрение получают путем смешения двойного суперфосфата, карбамида и хлористого калия. Какие массы ингредиентов нужно взять для выполнения условиях Х и заданном соотношении N : P : К, если:
– двойной суперфосфат содержит, мас. доля, %: СаНРО4 – 40,5; Са(Н2РО4)2 – 10,5;
– карбамид содержит, мас. доля, %: N – 45,5;
– хлористый калий содержит, мас. доля, %: KCl – 95,0.

Скачать решение задачи 2 (вар 1) (цена 70р)
Задача 4 (вар 1). При получении олеума содержащий SO3 газ с температурой 313 К орошается 20 %-ным олеумом с температурой 313 К. Определите количество подаваемого на орошение олеума при заданной степени абсорбции SO3, если теплота конденсации газообразного SO3 – 481,85 кДж/кг SO3, теплота растворения жидкого SO3 в 20 %-ном олеуме – 23,25 кДж/моль SO3, температура уходящего газа – 323 К, температура олеума на выходе – 328 К. Средняя теплоемкость олеума – 1,344 кДж/(м3 град), газа – 1,42 кДж/(м3 град), или 2,04 кДж/(кг град). Потерями тепла пренебречь.

Скачать решение задачи 4 (вар 1) (цена 70р)
Задача 5 (вар 1) Нитрозные газы с содержанием компонентов, об. доля, %: NО – 10; O2 – 8; N2 – остальное, направляются для осуществления реакции оксиления окиси азота до двуокиси азота по реакции
2NO + O2 = 2NO2,
кинетическое уравнение которой соответствует необратимой реакции 3-го порядка, в непрерывно действующий реактор идеального вытеснения при общем давлении 0,2 МПа с целью достижения степени превращения NO в NO2, равной 90% при объемной скорости нитрозных газов (при н. у.), равной 30 000 м3?ч. Рассчитать объем реактора, обеспечивающий указанный процесс, при условии, что его температура и численное значение константы скорости реакции, а также общее давление (в МПа) отвечают номеру примера из таблицы.
Для Варианта 5 условие задачи остается тем же, за исключением общего давления, равного 0,3 МПа.
Температура, 90 С, Значение константы скорости реакции 2*10^4
Скачать решение задачи 5 (вар 1) (цена 70р)
Вариант 2 пример 1
Задача 1 (вар 2) Определить продолжительность работы катионитового фильтра без регенерации до исчерпания обменной способности
1. Обменная емкость катионита, 800 моль-экв/м3
2. Объем катионита в фильтре, 25 м3
3. Объемный расход воды 65 м3/ч
4. Общая жесткость воды 4,8 ммоль экв/л
Скачать решение задачи 1 (вар 2) (цена 70р)
Задача 2 (вар 2) Тугоплавкое стекло получают путем сплавления шихты, состоящей из поташа, кальцита и кварцита. Состав тугоплавкого стекла задан:
– А (мас. доля, %): К2О – 18,4; СаО – 11,0; SiO2 – 70,6;
– Б (мольная доля): К2О – 0,11; СаО – 0,23; SiO2 – 0,66.
В каких массовых соотношениях нужно смешать ингредиенты, чтобы выполнить условие Х?
Состав ингредиентов, мас. доля, %:
поташ: К2СО3 – 95,0; SiO2 – 5,0;
кальцит: СаСО3 – 90,0; SiO2 – 10,0;
кварцит: SiO2 – 95,0; СаСО3 – 5,0.

Скачать решение задачи 2 (вар 2) (цена 70р)
Задача 3 (вар 2) Составить материальный баланс процесса получения азотной кислоты и рассчитать: а) выход оксида азота на поданный аммиак; б) теоретический и фактический расходные коэффициенты по сырью; в) состав газа после окисления аммиака. Расчет вести на часовую производительность газовоздушной установки на основе следующих реакций:
4NH3 + 5O2 = 4NO + 6H2O; (1)
4NH3 + 3O2 = 2N2 + 6H2O; (2)
2NO + 1,5 O2 + H2O = 2HNО3. (3)

Скачать решение задачи 3 (вар 2) (цена 70р)
Задача 4 (вар 2) Для выделения аммиака из азотоводородной смеси заданного состава ее охлаждают водой с температурой 293 К. Определите расход воды на получение 1000 кг аммиака при заданных степени конденсации аммиака, начальной и конечной температурах газа; конечная температура воды – 308 К; энтальпия жидкого аммиака – 170 кДж/кг.
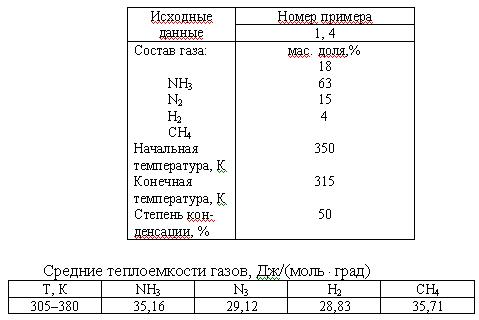
Скачать решение задачи 4 (вар 2) (цена 70р)
Задача 5 (вар 2) Нитрозные газы с содержанием компонентов, об. доля, %: NО – 10; O2 – 8; N2 – остальное, направляются для осуществления реакции оксиления окиси азота до двуокиси азота по реакции
2NO + O2 = 2NO2, (1)
кинетическое уравнение которой соответствует необратимой реакции 3-го порядка, в непрерывно действующий реактор идеального вытеснения при общем давлении 0,2 МПа с целью достижения степени превращения NO в NO2, равной 90% при объемной скорости нитрозных газов (при н. у.), равной 30 000 м3?ч. Рассчитать объем реактора, обеспечивающий указанный процесс, при условии, что его температура и численное значение константы скорости реакции, а также общее давление (в МПа) отвечают номеру примера из таблицы.
Для Варианта 5 условие задачи остается тем же, за исключением общего давления, равного 0,3 МПа.
Температура, 90 С, Значение константы скорости реакции 2*10^4
Скачать решение задачи 5 (вар 2) (цена 70р)
Задача Б1 Определить карбонатную, некарбонатную и общую жесткость воды заданного состава, а также массу фосфата натрия (Na3PO4 * 12H2O), необходимого для ее умягчения.

Скачать решение задачи Б1 (цена 70р)
Задача Б2 Рассчитать массу известкового молока и раствора соды, необходимых для умягчения воды известково-содовым способом.
1. Общая жесткость воды, 10,8 ммоль ? экв/л
2. Карбонатная жесткость, 5,4 ммоль ? экв/л
3. Массовая концентрация CO2, 15 мг/л
4. Массовая доля Са(ОН)2 в известковом молоке 6 %
5. Массовая доля соды 10 %
6. Объем умягчаемой воды 15000 м3
Скачать решение задачи Б2 (цена 70р)
Задача Б3. Определить карбонатную, некарбонатную и общую жесткость воды заданного состава. Массовые концентрации компонентов в воде: Са2+ 90 мг/л; Mg2+ 15 мг/л; НСО3- = 165 мг/л. Определить массу известкового молока и технической соды, необходимых для умягчения воды, если массовая доля Са(ОН)2 в известковом молоке 6 %, массовая доля Na2CO3 в технической соде 98 %. Объем умягчаемой воды 1000 м3.
Скачать решение задачи Б3 (цена 70р)
