Курсовые по ОХТ описание схем
Разработка математической модели кинетической реакции
Проводим разработку кинетической модели реакции, пример разработки
Возможно проведения исследования кинетики реакции по вашим данным!
Пример разобранной реакции
1 Исходные данные и подбор реакции
Исходные данные
Начальные концентрации:
• СА,0=0,5 моль/л = 500 моль/м3;
Значения констант скоростей при Т=580К:
• k1=0.2;
• k2=0.15;
Значения энергии активации:
• Е1=9,305*104 Дж/моль;
• Е2=10,1*104 Дж/моль;
Расход потока QV0=5590 л/ч = 0,00155 м3/с
Исходная схема:
 (1)
(1)
Для данной схемы были подобраны реакции термического разложения этанола
 (2)
(2)
Схема подобранных реакций
 (3)
(3)
Целевой компонент: этан (C2H6)
Кинетическая модель
На основании закона действующих масс составим уравнения для скорости реакции
По нашей модели по уравнениям (3) получим:

В Matlab вводим скорости реакций, константы химических реакций и начальные концентрации веществ.
x0 = [500 0 0]; % начальные концентрации веществ, моль/м3
t = [0 50];
[time,x]= ode45('kin',t,x0);
plot(time, x(:,1), time, x(:,2), time, x(:,3))
ylabel('концентрация, моль/м3');
xlabel('время, с');
legend ('Этанол','Этан','Кислород')
function y = kin(t,x)
k1 = 0.0002; % константа реакции второго порядка, 1/с
k2 = 0.00015; % константа реакции второго порядка, 1/с
r1 = k1*(x(1)^2);
r2 = k2*(x(2)^2)*x(3);
y = [r2-r1;r1-r2;r1-r2];
end
Время выбираем на промежутке от 0 до 50 секунд.
После ввода данных, имеем график зависимости концентрации веществ от времени:

Рис 2. График изменения концентраций веществ по времени.
Основная реакция по получению этана идет с разложением этанола [1]. Согласно анализу графика рис. 2 этан выделяется в максимальном количестве уже на первых секундах реакции до уровня 60 моль/м3. Для того, чтобы определить эффективность ректора идеального вытеснения с катализаторным комплексом необходимо составить график концентрации от длины реактора.
Гидродинамическая модель
Эта процесса представляет систему дифференциальных уравнений гидродинамики идеального вытеснения, записанную для каждого из компонентов реакционной смеси:

С позиций проектирования наиболее интересно исследование процесса при его стационарной реализации, то есть при:

Энергетическая модель
При исследовании работы реактора необходимо изучить особенности протекания реакций в широком диапазоне температур, то есть дополнить модель реактора частной энергетической моделью, учитывающей влияние температуры на константу скорости частной реакции в виде уравнения Аррениуса.
 (16)
(16)
где k – константа скорости реакции
v0 – предэкспоненциальный множитель
Еa – энергия активации, Дж/моль
R – универсальная газовая постоянная, Дж/моль×К
Т0 – начальная температура, К
При формировании полной модели с учетом энергетики процесса необходимо также учитывать зависимость скорости потока от температуры, связанную с изменением объема реакционной смеси.
В связи с тем, что все вещества являются газообразными в данных условиях, то используется следующая формула для скорости потока газа:
 (17)
(17)
w0- начальная скорость линейного потока, м/с
T- температура потока, К
w- линейная скорость потока, м/с
T0- начальная температура потока, К
Тепловой режим модели
Необходимо учитывать такой существенный фактор химического процесса, как теплота реакции, приводящая к разогреву или охлаждению реакционной смеси в реакторе.
Тепловые эффекты учитываются для рассматриваемой задачи частной тепловой моделью в форме дифференциального теплового баланса.
Реактор, в котором тепловые эффекты приводят к изменению температуры процесса и при этом отсутствует теплоперенос за пределы аппарата называется адиабатическим реактором.
Тепловая модель реактора описывается следующим уравнением:

Отсюда следует
 (18)
(18)
где υ - расход потока, м3/с
S- площадь поперечного сечения реактора, м3
ρ - плотность смеси, кг/м3
cp- Теплоемкость смеси, Дж/моль∙К
∆H1, ∆H2 – Энтальпии реакций, Дж/моль
Моделирование реактора
В качестве первого действия пересчитаем заданные при температуре 300 К константы скоростей реакций при действительных температурах протекания реакций (5-6) для создания энергетической модели реакций. Для этого в командном окне Матлаб вычислим соответствующие предэкспоненциальные коэффициенты по формуле
 (19)
(19)
где k0 – константа скорости при температуре Т0,
Еа – энергия активации (Дж/моль),
R – универсальная газовая постоянная (8,31 Дж/моль/К)

Результат расчета


Присвоим каждому компоненту системы порядковый номер для обозначения в расчетах:
• этанол – 1
• этан – 2
• кислород – 3
Таблица 1 - значения коэффициентов a, b и c для пересчета теплоемкостей компонентов реакционной смеси, а также формулы для расчета теплоемкостей веществ при определенной температуре.
 (20,21)
(20,21)
где a, b, c – константы пересчета теплоемкости при температуре Т (К), отличной от нормальных условий.
Таблица 1
Значения энтальпий веществ и коэффициентов a, b и с
|
Компонент |
ΔH0298, кДж/моль |
a |
b*103 |
c*10-6 |
|
Этанол |
-276,98 |
10,99 |
204,7 |
-74,2 |
|
Этан |
-84,67 |
5,75 |
175,11 |
-57,85 |
|
Кислород |
0 |
31,46 |
3,39 |
-3,77 |
Для создания тепловой модели системы реакций рассчитаем теплоемкость смеси (20-21), предварительно вычислив мольные доли каждого из компонентов системы как отношение концентраций соответствующих компонентов к сумме всех концентраций смеси по формуле
 (22)
(22)
где fi – мольные доли компонентов,
xi – концентрации компонентов, моль/м3.
 (23)
(23)
Cp – теплоемкость смеси, Дж/К,
cpi– теплоемкости компонентов, Дж/К.
В качестве следующего действия запишем уравнения для расчета энтальпии каждого из веществ, значения энтальпий и коэффициентов представлены в таблице 1.
 (24)
(24)
 - энтальпия компонентов при температуре Т(К),
- энтальпия компонентов при температуре Т(К),
 – энтальпии компонентов при нормальных условиях,
– энтальпии компонентов при нормальных условиях,
 – теплоемкости компонентов, Дж/К.
– теплоемкости компонентов, Дж/К.

Подставим полученные значения теплоемкостей, а также значения энтальпий при 298 К – ΔH0298 в уравнения расчета энтальпии каждого из веществ, затем при помощи полученных значений вычислим суммарную энтальпию каждой реакции как разность энтальпий продуктов и реагентов
Проведем выбор аппарата по адиабатным условиям



Рис. 3 График для адиабатных условий
При выполнении процесса при адиабатных условиях для реактора типа РИВ рис. 3, оптимальная температура процесса проведения реакции падает до 300К резко, что говорит о поглощении тепла реакцией в большом количестве в начальный момент времени. Процесс не стабилен, так как температура устанавливается только на длине 0,3 м, при этом максимальный выход этана остается на максимальном уровне 60 моль/м3.
Проведем выбор аппарата по политропным условиям
Рассмотрим политропный реактор с греющей рубашкой и температурой теплоносителя 600 К.
Коэффициент теплопередачи возьмём равным 200 Вт/м2*К, что типично для органических газов.
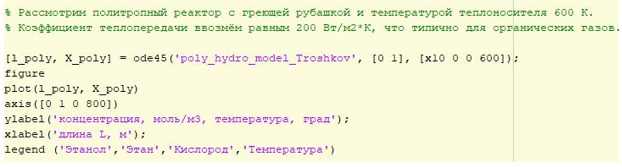
Уравнение теплового баланса для политропного режима
 (25)
(25)
K - коэффициент теплопередачи в реакторе Вт/м2 К.
Th - температура внешнего теплоносителя, К.


Рис. 4 График для политропных условий
При выполнении процесса при политропных условиях рис. 4, видно, что температура за счет дополнительного подогрева увеличилась до 390 К при этом реакции осуществима мгновенно, минимальная эффективная длина реактора составляет 0,1м, выход этана максимальный и соответствует кинетической модели анализа.
Вывод: в результате проведения тепловых параметров процесса оптимальным является политропный режим, так как при адиабатном не достигается стационарность процесса из-за поглощения теплоты реакцией.
Выводы
На основании исходных данных по схеме реакции подобраны целевые реакции разложение этанола до этана. Произведен выбор аппарата идеального вытеснения РИВ и на основе действующего производства выбрана и описана кинетическая модель реактора.
По выбранным данным произведен расчет реактора в программе «MatLab» в результате составления программы получаем цилиндрический политропный реактор с подобранным диаметром d = 0,15м, длина реактора L = 0,1м. Выход целевого вещества этана 60 моль/м3.
Выполняем разработку технологических процессов механической обработки детали
Выполняем разработку технологических процессов и маршрутных процессов получения цилиндрических деталей в среде Вертикаль (версия 13, 14) под ваше оборудование и задачи.
Пример выполненного тех процесса в среде Вертикаль
Имеется вот такое Кольцо 3D


По нему разработан чертеж детали с требованиям форм и расположения паза и выступов (шипов)

Скачать чертеж Кольца в pdf(209.53 Кб) скачиваний8 раз(а)
Для начала разберем маршрут технологии. Так как деталь имеет тело вращения, то наиболее востребованным будет использовать токарный станок средних размеров с функцией С-ось (это минимально требование для получения паза и выступов), если будет полноценная Y координата, будет еще лучше, то есть нам нужен 4-х осный станок. Подбираем тип станка, например, GOODWAY

Таким образом, для обработки детали достаточно будет двух токарных операций с каждой стороны и фрезерная обработка паза, базирование детали в трехкулачковом (можно в цанговом) патроне. Все схемы базирования и маршрут обработки с оснасткой приведены ниже.
Рассмотрим технологию обработки
Операция 005 Заготовительная (ленточнопильный станок)
1 Отрезать прутки в размер 800…1000 мм (в зависимости от исходного пруткового проката)
Операция 010 Слесарная (Точильный станок)
2 Заправить прутки фаской (это необходимо, чтобы прутки не застревали при подаче их в барфидере.
Операция 015 Токарная с ЧПУ (GOODWAY)
1. Загрузить прутки в загрузочное устройство
2. Подрезать торец "как чисто"
PCLNR 2020K12 Державка
CNMG 120404-РМ 4225 Пластина
3. Точить поверхности 4 и 5, выдерживая размер 1, с притуплением острой кромки фаской в размер 9
PCLNR 2020K12 Державка
CNMG 120404-РМ 4225 Пластина
ШЦ-I-125-0,02 Штангенциркуль ГОСТ 166-89
4. Сверлить отверстие ф17мм, на длину L=12мм, за два вывода
2300-0237 Сверло ф17 ГОСТ 10902-77
880-0202 W05HP-LM4044 Пластина
880-0202 04H-C-LM1044 Пластина
ШЦ-I-125-0,05 Штангенциркуль ГОСТ 166-89
5. Расточить поверхности 2 и 3, выдерживая размер 1, с притуплением острой кромки фаской в размер 9
А10-SCLCR 06 Державка
CCMT 060204-PF Пластина
8367-0793 Калибр для контроля длины стоек
8133-0939 Пробка ф25+0,21
6. Фрезеровать выступы, выдерживая размеры 1, 8, 10
GM-4EL-10 Фреза концевая ф10
ШЦ-I-125-0,05 Штангенциркуль ГОСТ 166-89
8371-1076 Калибр на симметричность
7. Отрезать деталь, выдерживая размер 1 и 7, с притуплением острой кромки фаской 0,3х45
QEED 2020R17 Державка
ZPED 02502-MG-15R YBG302 Пластина
ШЦ-I-125-0,05 Штангенциркуль ГОСТ 166-89

Операция 020 Токарная с ЧПУ (GOODWAY)
1. Установить и снять деталь в трехкулачковый патрон
2. Расточить поверхность 1, выдерживая размер 2, с притуплением острой кромки фаской 0,3х45°
А10-SCLCR 06 Державка
CCMT 060204-PF Пластина
8133-0945 Пробка 30,2+0,16

Операция 025 Фрезерная (Фрезерный станок СФ-676)
1. Установить и снять деталь в кассету по 6 шт.
7210-1471 Приспособление фрезерное
2. Фрезеровать паз, выдерживая размер 1
6222-0037 Оправка
Набор фрез
8371-1075 Калибр на симметричность
ШЦ-I-125-0,1 Штангенциркуль ГОСТ 166-89

Операция 030 слесарная (Точильно-шлифовальный станок ТШ-1)
1. Притупить заусенцы после фрезерования фаской 0,3х45, согласно, эскизу и контрольному образцу
2826-0026 Надфиль ГОСТ 1513-77
Контрольный образец

Операция 035 Контроль
Стол СТК
1. Проверить внешний вид детали, наличие фасок и притуплений, шероховатость Контрольный образец
2. Первую отладочную деталь проверить с использованием специального измерительного проектора
3. Проверить размеры
1, 3, 6, 7, 8, 9 - 5% контроля от партии
ШЦ-I-125-0,02 Штангенциркуль ГОСТ 166-89
2 - 10% контроля от партии
8133-0945 Пробка 30,2+0,
4, 5 - 10% контроля от партии
Калибр для контроля длины
10 - 5% контроля от партии
8133-0939 Пробка ф25+0,21
11 - 5% контроля от партии
Калибр на симметричность

Скачать карты ведомости оснастки в pdf(23.83 Кб) скачиваний9 раз(а)
Скачать карты эскизов в pdf(1.19 Мб) скачиваний8 раз(а)
Скачать карту контроля в pdf(22.23 Кб) скачиваний9 раз(а)
Скачать карты операций в pdf(49.97 Кб) скачиваний9 раз(а)
Скачать маршрутную карту оснастки в pdf(28.47 Кб) скачиваний8 раз(а)
Скачать титульный лист в pdf(12.83 Кб) скачиваний10 раз(а)
Задача 1
1.1. Производство уксусное кислоты жидкофазным окислением бутана
1.2. Производство фенола окислением толуола (Cкачать работу цена 450р)
1. Привести технологическую классификацию реакций, положенной в основу способа производства химического продукта; назвать объекты управления, перечислить основные группы факторов, используемых для оптимизации показателей процесса.
По этому новому методу фенол может быть получен двухстадийным окислением толуола сначала в бензойную кислоту, а затем в бензоилсалициловую кислоту, которая при гидролизе дает фенол и бензойную кислоту, возвращаемую на вторую стадию окисления.
Толуол окисляется кислородом воздуха в среде уксусной кислоты при 70-90°С в присутствии ацетата кобальта
2. Температурный режим работы реактора окисления толуола
Окисление толуола в бензойную кислоту проводят при температуре 120-150°, в следствии чего в реакционном аппарате создается избыточное давление до 2,5 атм. Эта величина определяется парциальным давлением...
Тепловой режим работы реактора окисления толуола
Толуол, воздух и катализатор подают в реактор 1, где происходит окисление химическая реакция окисления...
Гидродинамический режим работы реактора окисления толуола
Реактор представляет собой барботажную колонну. При барботаже часть газа вследствие трения распыляется ...
3. Указать класс технологической схемы, её достоинства и недостатки
Схема производства фенола из толуола приведена на рис. 3.1. Толуол, воздух и катализатор (нафтенат кобальта) подают в реактор 1, где происходит окисление толуола в жидкой фазе. Температура в реакторе поддерживается около 150 °С
4. Начертить функциональную схему процесса, структурную схему реакторного блока и операторную схему одной из подсистем.
Рисунок 4.1 – Функциональная схема процесса получения фенола окислением толуола.
Рисунок 4.2 - Операторная схема подсистемы получения бензойной кислоты
Рисунок 4.3 – Структурная схема реакторного блока
5. Выполнить экологическую экспертизу технологической схемы и дополнить функциональную схему подсистемами экологизации производства, как она вам представляется.
Рассматривая схему 3.1 производства фенола окислением толуола с точки зрения экологизации можно применить следующие подсистемы:
- после отстойника 3 можно применить комплексную очистку воды и применения ее на технологические нужды....
6. Выполнить энергетическую экспертизу ХТС фенола окислением толуола
Анализ схемы производства фенола из толуола на рис. 3.1 выявлены следующие пути повышения энергетической эффективности ХТС:
1) Рекуперация тепла в реакторе 1, а также ...
1.3. Производство уксусной кислоты окислением н-бутенов (Cкачать работу цена 450р)
1. Привести технологическую классификацию реакций, положенной в основу способа производства химического продукта; назвать объекты управления, перечислить основные группы факторов, используемых для оптимизации показателей процесса.
Технологическая классификация реакций
Промышленные установки по получению уксусной кислоты этим методом имеются в США, Англии, ФРГ и других странах. В России процесс жидкофазного окисления н-бутана разработан Н. М. Эммануэлем...
Гидродинамический режимов работы реактора уксусной кислоты окислением н-бутенов
Соотношение скоростей распада перекисного радикала и взаимодействия образующихся при распаде алкоксильных радикалов с н-бутаном при жидкофазном процессе
Температурный режим работы реактора уксусной кислоты окислением н-бутенов
Окисление н-бутана проводится при 140- 170°С и 52 кгс/см2 (5,1 МН/м2), массовом отношении свежий
Тепловой режим работы реактора уксусной кислоты окислением н-бутенов
Энергия активации при гомогеннокаталитическом окислении углеводородов в жидкой фазе
3. Указать класс технологической схемы, её достоинства и недостатки
Свежий жидкий н-бутан подаемся и смеситель 1, куда поступают циркулирующий н-бутан из емкости 11 и «кислый н-бутан» из емкости 19. Смесь свежего и циркулирующего
5. Выполнить экологическую экспертизу технологической схемы и дополнить функциональную схему подсистемами экологизации производства, как она вам представляется.
Выделение уксусной кислоты в виду большого количества примесей может осуществляться только в двухкратной ректификационной установке и отпарного аппарата с последовательных выведением примесей
6. Выполнить энергетическую экспертизу ХТС уксусной кислоты окислением н-бутенов
Жидкофазное окисление н-бутана при температуре, близкой к критической, малоэффективно из-за небольшой...
1.4. Производство акриловой кислоты опадением прошивке
1.5. Производство винилацетата
Задача 2
2.1. Производство акролеина окислением пропилена (Cкачать работу цена 450р)
1. Привести технологическую классификацию реакции, положенной в основу способа производства химического продукта; назвать объекты управления, перечислить основные группы факторов, используемых для оптимизации показателей процесса.
Окисление пропилена в акролеин сопровождается выделением тепла (2110 ккал на 1 кг акролеина); при полном окислении пропилена в двуокись углерода и воду выделяется 11 390 ккал на 1 кг пропилена. ..
Тепловой режим реактора окислением пропилена
Реакцию проводят в разных реакторах..
Гидродинамический режим окислением пропилена
Процесс сопровождается образованием побочных веществ: ацетальдегида, ацетона, уксусной и акриловой кислот..
3. Указать класс технологической схемы, ее достоинства и недостатки.
Процесс сопровождается образованием побочных веществ: ацетальдегида, ацетона, уксусной и акриловой кислот, СО и СО2. Оксиды углерода, как обычно при гетерогенно-каталитическом окислении..
4. Начертить функциональную схему процесса, структурную схему реакторного блока и операторную схему одной их подсистем.
1) функциональная схема процесса:
2) структурная схема реакторного блока:
3)операторная схема подсистем подготовки сырья и химического превращения (реакторного блока)
где 1 – реактор;..
5. Выполнить экологическую экспертизу технологической схемы акролеина окислением пропилена
Созданию любого производства предшествует анализ альтернативных химических способов получения целевого продукта из заданного сырья или различных видов сырья, и в каждом конкретном случае оценивается степень безотходности способа...
6. Выполнить энергетическую экспертизу химико-технологической системы (ХТС) акролеина окислением пропилена
Рассматриваемая химико-технологическая система процесса получения акролеина с точки зрения энергетической эффективности относится к технологическим схемам...
2.2. Производство ацетальдегида окислением этилена (Cкачать работу цена 450р)
1. Привести технологическую классификацию реакций
В последнее время большое распространение получил способ получения ацетальдегида на базе этилена...
Гидродинамический режим реактора ацетальдегида окислением этилена
Выход ацетальдегида в зависимости от условий проведения реакций и состава катализатора колеблется в пределах 84-98%. При этом в качестве побочных продуктов...
Тепловой режим реактора ацетальдегида окислением этилена
В жидкофазном процессе тепло отводится за счет испарения продуктов синтеза и воды в токе газа. При этом из зоны реакции выводится ацетальдегид. Таким образом, в одностадийном способе процесс проводится при t=90-100°С и Р=1 МПа...
Температурный режим реактора ацетальдегида окислением этилена
Процесс проводят при 3-7 ат и 100-120° С. Образующиеся продукты вместе с раствором отработанного катализатора из верхней части реактора перетекают в сепаратор...
3. Указать класс технологической схемы, ее достоинства и недостатки.
В одностадийном варианте производства ацетальдегида из этилена все реакции проводятся в одном реакторе колонного типа. Технологическая схема представлена на рис. 3.1.
Рисунок 4.1 - Функциональная схема производства альдегидов карбонилированием пропилена
Рисунок 4.2 – Операторная схема производства альдегидов карбонилированием пропилена
Рисунок 4.3 – Структурная схема реакторного блока
5. Выполнить экологическую экспертизу технологической схемы ацетальдегида окислением этилена
Получение ацетальдегида из этилена более предпочтителен, прежде всего из-за того, что растворенные газы сразу отделяются от продуктов в колонне с обратным конденсатором. Вместе с тем в этом способе все ректификационные колонны обогреваются «острым паром»....
6. Выполнить энергетическую экспертизу ХТС ацетальдегида окислением этилена
Парофазный процесс прямого окисления этилена может быть только одностадийным, причем так же, как и в случае парофазного процесса, на основе ацетилена он может...
2.3. Производство синтетических жирных кислот окислением парафина
2.4. Производство изопрена из 2-метилпропена и формальдегида (Cкачать работу цена 450р)
1. Привести технологическую классификацию реакций
Способ получения изопрена из 2-метилпропена и формальдегида, разработанный впервые в нашей стране и уже освоенный промышленностью, состоит из двух стадий:
Гидродинамический режим реактора изопрена из 2-метилпропена и формальдегида
При взаимодействии изобутена с формальдегидом (реакция Принса) при более высокой температуре ...
Тепловой режим реактора изопрена из 2-метилпропена и формальдегида
Вторая стадия - расщепление 4,4-диметил-1,3-диоксана - идет с поглощением тепла 30 ккал/моль (126 кДж/моль). Подвод тепла может быть организован разными ...
Температурный режим реактора изопрена из 2-метилпропена и формальдегида
Первая стадия проводится в жидкой фазе при температуре 85-95°С в присутствии серной кислоты (концентрация Н3SО4 в растворе 1-1,5%), избирательность по формальдегиду ...
3. Указать класс технологической схемы, ее достоинства и недостатки.
Схема производства изопрена приведена на рис. 3.1. Процесс конденсации проводится в двух последовательно соединенных реакторах. Изобутан-2-метилпропеновая ...
Рисунок 4.1 - Функциональная схема процесса получения изопрена
Рисунок 4.2 – Операторная схема подсистемы выделения изопрена
Рисунок 4.3 Схема реакторного блока
5. Выполнить экологическую экспертизу технологической схемы изопрена из 2-метилпропена и формальдегида
При выполнении анализа экологизации схемы можно выделить два основных узла системы очистки: первый - это очистка газовых выбросов, второй – очистка сточных вод...
6. Выполнить энергетическую экспертизу ХТС изопрена из 2-метилпропена и формальдегида
Вторая стадия - расщепление 4,4-диметил-1,3-диоксана - идет с поглощением тепла 30 ккал/моль (126 кДж/моль). Подвод тепла может быть организован разными ...
2.5. Производство алкилбензолов
Задача 3
3.1 Производство вторичных алкилосульфатов (Cкачать работу цена 450р)
1. Привести технологическую классификацию реакций
Олефины охлаждают до 5°С и при сильном перемешивании и охлаждении обрабатывают серной кислотой. Образуются моно- и диалкилсульфаты...
Гидродинамический режим реактора вторичных алкилосульфатов
Неразветвленные бутилены и амилены, например н-бутилен, н-амилен, псевдобутилен СН3—СН=СН—СН3, а также амилен СН3—СН=СН—С2Н8, образуют с 75—80%-ной ...
Тепловой режим реактора вторичных алкилосульфатов
Образованию диалкилсульфатов способствует повышение давления и концентрации кислоты, а также избыток олефина (увеличение соотношения олефин: кислота). Диалкилсульфаты ...
Температурный режим реактора вторичных алкилосульфатов
Повышение температуры, способствующее образованию алкилсульфатов, одновременно ускоряет и реакции полимеризации. Интенсивность полимеризации олефина зависит от его молекулярного веса...
3. Указать класс технологической схемы, ее достоинства и недостатки.
Олефины охлаждают до 5°С и при сильном перемешивании и охлаждении обрабатывают серной кислотой. На второй стадии (нейтрализация)...
Рисунок 4.1 - Функциональная схема получения алкилосульфатов
Рисунок 4.2 – Операторная схема получения алкилосульфатов
Рисунок 4.3 – Структурная схема реакторного блока вторичных алкилосульфатов
5. Выполнить экологическую экспертизу технологической схемы
Рассматривая технологическую схему производства олефина можно выделить основные вредный факторы воздействующие на экологическую систему:
1) Использование серной кислоты...
6. Выполнить энергетическую экспертизу ХТС вторичных алкилосульфатов
Схема производства алкилосульфатов не использует для производства больших затрат энергии. Но существующую схему возможно усовершенствовать за счет использующегося тепла реакции...
3.2 Производство высших жирных спиртов гидрированием синтетических жирных кислот (Cкачать работу цена 450р)
1. Привести технологическую классификацию реакций
В настоящее время в мировой практике для получении высших жирных спиртов фракции С10 С20 широко используется процесс восстановления жирных кислот или их эфиров...
Гидродинамический режим реактора высших жирных спиртов гидрированием синтетических жирных кислот
С точки зрения экономических показателей более эффективным оказывается процесс с применением цинкхромового катализатора. В этом случае потребуется...
Тепловой режим реактора высших жирных спиртов гидрированием синтетических жирных кислот
В начальный период окисление проводят осторожно, при интенсивном охлаждении...
Температурный режим реактора высших жирных спиртов гидрированием синтетических жирных кислот
Реакцию проводят при 60-70° С и 10 ат. Образующийся три-этилалюминий частично возвращают на получение диэтилалюми-нийгидрида...
3. Указать класс технологической схемы, ее достоинства и недостатки.
Этерификация синтетических жирных кислот. Этерификация смеси жирных кислот может осуществляться различными спиртами. В промышленной практике ...
Рисунок 4.1 - Функциональная схема процесса получения высших жирных кислот
Рисунок 4.2 – Операторная схема подсистемы получения высших жирных кислот
Рисунок 4.3 Схема реакторного блока высших жирных спиртов гидрированием синтетических жирных кислот
5. Выполнить экологическую экспертизу технологической схемы высших жирных спиртов гидрированием синтетических жирных кислот
Рафинация эфиров заключается в удалении не вступивших в реакцию синтетических жирных кислот. Сырой эфир непосредственно из этерификатора или со склада подается и нейтрализатора
6. Выполнить энергетическую экспертизу ХТС высших жирных спиртов гидрированием синтетических жирных кислот
При анализе технологической схемы получения высших жирных видно что наиболее энергоемкое отделения является ректификационная установка. Для наиболее эффективного
3.3 Производство высших жирных спиртов восстановлением метиловых эфиров первичных спиртов (Cкачать работу цена 450р)
1. Привести технологическую классификацию реакций
В настоящее время в мировой практике для получении высших жирных спиртов фракции С10 С20 широко используется процесс восстановления жирных кислот или их эфиров...
Гидродинамический режим реактора высших жирных спиртов восстановлением метиловых эфиров первичных спиртов
С точки зрения экономических показателей более эффективным оказывается процесс с применением цинкхромового катализатора. В этом случае потребуется...
Тепловой режим реактора высших жирных спиртов восстановлением метиловых эфиров первичных спиртов
В начальный период окисление проводят осторожно, при интенсивном...
Температурный режим реактора высших жирных спиртов восстановлением метиловых эфиров первичных спиртов
Реакцию проводят при 60-70° С и 10 ат. Образующийся три-этилалюминий частично возвращают на получение диэтилалюми-нийгидрида; остальное...
3. Указать класс технологической схемы, ее достоинства и недостатки.
Технологическая схема процесса прямого гидрировании на стационарном меднохромовом катализаторе приведена па рис. 1). Кислоты из сырьевой емкости в насосом 5 и сложи К водород компрессором 3...
Рисунок 4.1 - Функциональная схема процесса получения высших жирных кислот
Рисунок 4.2 – Операторная схема подсистемы получения высших жирных кислот
Рисунок 4.3 Схема реакторного блока высших жирных спиртов восстановлением метиловых эфиров первичных спиртов
5. Выполнить экологическую экспертизу технологической схемы высших жирных спиртов восстановлением метиловых эфиров первичных спиртов
При выполнении анализа экологизации схемы можно выделить два основных узла системы очистки: первый - это очистка газовых выбросов, второй – очистка сточных
6. Выполнить энергетическую экспертизу ХТС высших жирных спиртов восстановлением метиловых эфиров первичных спиртов
При анализе технологической схемы получения жирных кислот можно выделить реакторный узел, как наиболее энергоемкий процесс. Для его усовершенствования
3.4 Производство а-олефинсульфонатов
3.5 Производство глицерина из аллилового спирта и надуксусной кислоты (Cкачать работу цена 450р)
1. Привести технологическую классификацию реакций
Видоизменениями классического метода Вильямса являются трехстадийный синтез глицерина по схеме Сложная, необратимая...
Гидродинамический режим реактора а-олефинсульфонатов
Отношение пропилена к кислороду по весу 4: 1
Температура в контактном аппарате 300 - 400°С
Давление 1 - 10 атм...
Тепловой режим реактора а-олефинсульфонатов
Температура в контактных аппаратах 60 - 70°С, поддерживается за счет подачи пара в рубашку или теплой воды. С учетом эндотермической реакции необходимо постоянно контролировать...
Температурный режим реактора а-олефинсульфонатов
Для осуществления процесса ректификации жидкой фазы необходимо необходимо подача острого...
3. Указать класс технологической схемы, ее достоинства и недостатки.
Получение глицерина из аллилового спирта и надуксусной кислоты осуществимо по описываемой ниже схеме (рис. 3.1).
Рисунок 4.1 - Функциональная схема получения глицерина
Рисунок 4.2 – Операторная схема получения глицерина
Рисунок 4.3 – Структурная схема реакторного блока а-олефинсульфонатов
5. Выполнить экологическую экспертизу технологической схемы а-олефинсульфонатов
При производстве глицерина возникает проблема с очисткой отходящих газов, так как они содержат смолы и продукты реакции глицерина.
Способ очистки газов заключается ...
6. Выполнить энергетическую экспертизу ХТС а-олефинсульфонатов
Схема производства глицерина использует для производства больших затрат энергии. При рассмотрении реактора можно выделить рубашку реактора с теплоносителем...
Cтраница 1 из 3


